انضم إلى منتدى المصممين
خبرتك ضرورية للمجتمع. انضم إلينا وساهم بمعرفتك
انضم إلى المنتدى الآنشارك وتعلّم وتقدّم مع أفضل المحترفين في هذا المجال
المعادن هي عناصر طبيعية فريدة من نوعها تمتلك خصائص كل من المعادن والخلايا. خصائصها المميزة تجعل المعادن لا يمكن الاستغناء عنها في سيناريوهات مختلفة. تستكشف هذه المقالة هذه المجموعة من العناصر ، وتناقش خصائصها وتطبيقاتها ومواقفها في الجدول الدوري. سنقدم أيضًا لمحة موجزة عن كل ميتولويد معترف به بشكل شائع.
- معرض المعادن الخصائص التي هي مزيج من كل من المعادن والمعادن، مما يجعلها متعددة الاستخدامات لمجموعة واسعة من التطبيقات العامة والمتخصصة.
- يشغلون أ خط متعرج في الجدول الدوري. تقع المعادن على جانب واحد من هذه المنطقة القطرية ولا تقع غير الممتلكات على الجانب الآخر. يشير هذا الترتيب أيضًا إلى خصائصها الهجينة.
- المعادن تحمل كبيرة أهمية في التكنولوجيا، خاصة في تصنيع أشباه الموصلات. أشباه الموصلات هي مكونات أساسية في أجهزة الكمبيوتر والإلكترونيات والألواح الشمسية.
- بعض metalloids ، مثل التيلوريوم وأنتيمون ، تحمل كبير الأهمية الاقتصادية والاستراتيجية بسبب ندرتهاوالتي يمكن أن تؤثر بشدة على الدفاع وإنتاج الطاقة وصناعات السيارات.
ما هي المعادن؟
المعادن هي عناصر مميزة امتلاك خصائص وسيطة بين المعادن والمعادن. وتشمل هذه الخصائص الوسيطة الكهربية والكثافة وطاقة التأين والقوة والتوصيل الحراري ونقطة الانصهار والتوصيل الكهربائي.
المجموعة المحددة من الخواص الفيزيائية والكيميائية والميكانيكية الموجودة في المعادن تجعلها مثالية للتطبيقات المتخصصة ، مثل أشباه الموصلات وتوليد الطاقة الشمسية. بالإضافة إلى ذلك ، يتم استخدامها على نطاق واسع في مختلف التطبيقات العامة ، بما في ذلك الأدوية ومبيدات الأعشاب والمبيدات الحشرية.
أحد أسباب الخصائص المتوسطة للمعادن هو عدد إلكترونات التكافؤ في قشرةها الخارجية. عادةً ما تمتلك المعادن إلكترونات واحدة إلى ثلاثة إلكترونات في قشرةها الخارجية ، في حين أن غير الممتلكات لها أربعة إلى سبعة. تحتوي المعادن على ثلاثة إلى ستة إلكترونات في قشرة التكافؤ ، مما يتيح لهم تكوين مركبات intermetallic مع المعادن (الروابط الأيونية) والسندات التساهمية مع nonmetals.
تحدد بعض المصادر ستة عناصر معدنية ، بينما يتعرف البعض الآخر على ثمانية عناصر. تشمل العناصر المعترف بها بشكل شائع في المجموعة المعدنية بورون (ب) ، الزرنيخ (AS) ، السيليكون (SI) ، الأنتيمون (SB) ، البولونيوم (PO) ، التيلوريوم (TE) ، الجرمانيوم (GE) ، والأستاتين (AT).
المعادن على الجدول الدوري
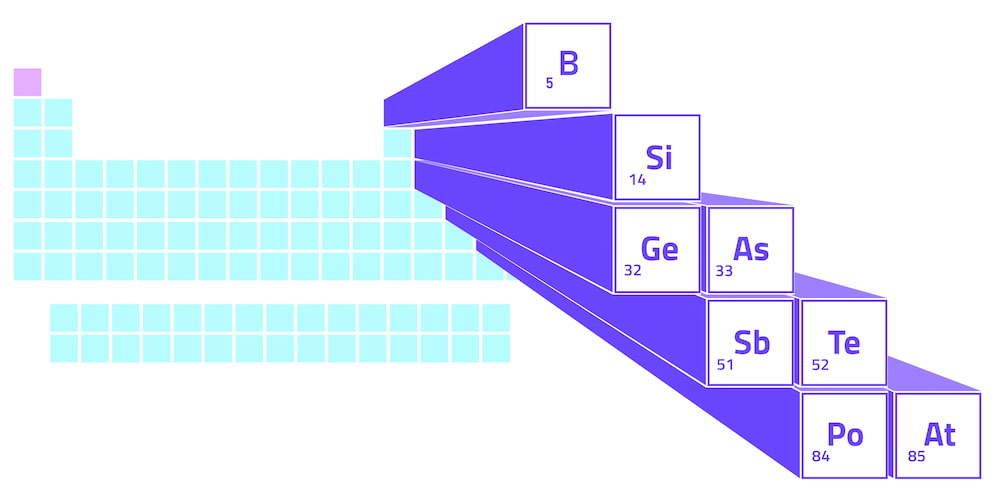
metalloids شكل أ خط متعرج في كتلة P للجدول الدوري ، وهو القسم المرتفع على الجانب الأيمن من الجدول. يبدأ خط التعرج هذا في بورون في المجموعة 13 ، ويتحرك قطريًا إلى السيليكون ، ثم يستمر بطريقة تشبه الخطوة إلى أستاتين في المجموعة 17. تشير المجموعات إلى ترقيم الأعمدة في الجدول الدوري.
على الجانب الأيسر من خط المعادن المتعرج ، نجد المعادن (باستثناء الهيدروجين). على الجانب الأيمن ، لدينا nonmetals. لذلك ، و المعادن تخلق خطًا تقسيمًا بين المعادن والمعادن في الجدول الدوري.
الخصائص العامة للمعادن
تظهر المعادن مزيجًا فريدًا من الخصائص غير الموجودة في عناصر أخرى. بعض هذه الخصائص تشمل:
الموصلية الكهربائية المتغيرة
الموصلية الكهربائية للمعادن الوسيطة ، تسقط بين المعادن والمعادن. ويعزى ذلك إلى هياكل النطاق الإلكترونية الخاصة بهم ، والتي تشبه هياكل نصف الموصلات أو أشباه الموصلات.
ومع ذلك ، يمكننا تعزيز الموصلية من خلال تعاطي المنشطات. تتيح هذه العملية إنشاء مكونات إلكترونية أساسية ، مثل الثنائيات والترانزستورات والدوائر المتكاملة ، والتي تعتبر أساسية للحوسبة الحديثة.
مظهر
المعادن لها مظهر معدني وهي صلبة في درجة حرارة الغرفة. غالبًا ما تؤدي أسطحها اللامعة العاكسة إلى التعرف الخاطئ كمعادن. هذا اللمعان المعدني هو أيضًا السبب وراء أصل اسمهم ؛ المعادن يعني تشبه المعادن في اللاتينية/اليونانية.
الموصلية الحرارية
تظهر المعادن الموصلية الحرارية المعتدلة ، وهي أعلى من غير المعادن ولكنها أقل من المعادن. حتى بين المعادن الثمانية ، تختلف الموصلية الحرارية بشكل كبير. بعض المعادن هي موصلات حرارة فعالة ، في حين أن البعض الآخر يعمل كعوازل مثالية تقريبًا. تتيح هذه الخاصية استخدام بعض المعادن في الأجهزة الحرارية.
هشاشة
على عكس المعادن ، لا تتمتع المعادن بالخصائص الفيزيائية من اللياقة والقدرة على التحرير. أنها تنكسر بسهولة وتفتقر إلى القوة المطلوبة للتطبيقات الهيكلية.
التفاعل الكيميائي
المعادن تفاعلية إلى حد ما مع المعادن والخلايا. هم شائع في السبائك المعدنية كمضافات ل تعزيز خصائص المعادن الانتقالية ، مما يوفر فوائد مثل زيادة القوة وتحسين مقاومة التآكل.
مع غير المعادن ، تشكل المعادن روابط تساهمية من خلال مشاركة الإلكترونات. تفاعلاتهم مع مركبات الهالوجينات مثل Trifluoride Boron ، وثلاثي أكسيد الأنتيمون ورباعي البتات السيليكون.
المعادن المشتركة وتطبيقاتها
جميع المعادن تشترك في بعض الخصائص المشتركة. ومع ذلك ، على عكس مجموعات أخرى من العناصر مثل الهالوجينات ، والمعادن القلوية ، أو المعادن الأرضية القلوية ، يمتلك كل ميتالويد أيضًا خصائص فريدة. يسمح هذا التنوع باستخدام المعادن في مجموعة واسعة من التطبيقات.
بورون (ب)
بورون هو معدني أسود ولطيف يشكل حوالي 0.001 ٪ من قشرة الأرض بالوزن. إنه أصعب من جميع المعادن والعروض مقاومة حرارة ممتازة. تبلغ قيمة صلابة MoHS 9.3 ، مقارنة بـ 10 لـ Diamond ، وهي أصعب مادة معروفة.
Boron عنصر متعدد الاستخدامات مع مجموعة من التطبيقات. واحدة من هذه هي إنتاج زجاج البورسليكات ، كوب خاص مع ارتفاع الحرارة والمقاومة الكيميائية. كما أنه يستخدم لإنتاج مثبطات اللهب ومستحضرات التجميل والمبيدات الحشرية والمنظفات.
تُستخدم سبائك النيكل بورون كسبائك رئيسية لتشكيل سبائك مثل Superalloys المستندة إلى النيكل والفولاذ الخاص وسبائك اللحام.
البورون هو أيضا مفيدة في المنشطات السيليكون. يمكّننا المنشطات من إنتاج أشباه الموصلات القائمة على السيليكون والتي لا غنى عنها للحوسبة الحديثة.
السيليكون (SI)
السيليكون هو المعادن الأكثر شهرة و ثاني أكثر العناصر وفرة على الأرض، بعد الأكسجين. أنها تشكل حوالي 27 ٪ من قشرة الأرض بالوزن.
إنه خامل بشكل عام في درجات الحرارة المحيطة ، ومع ذلك ، تزداد تفاعلها مع درجة الحرارة. فهو يجمع بين الأكسجين لتشكيل السيليكا (ثاني أكسيد السيليكون) ، والذي يوجد في معظم الطين والصخور والرمال والتربة. فهو يجمع بين معظم المعادن والسبائك المعدنية ، مما ينقل الخواص مثل السيولة ومقاومة التآكل والقوة ومقاومة الحرارة.
السيليكا والسيليكون النقي هي مواد أساسية في الحوسبة الحديثة. يستخدم السيليكا لإنتاج المكثفات التي تخزن الطاقة الكهربائية في الدوائر. السيليكون ، الذي يستخدم للتصنيع مكونات الرقائق الإلكترونية الحرجة، يسمح لنا بإنشاء أجهزة إلكترونية أصغر وأسرع وأكثر قوة.
الجرمانيوم (GE)
مباشرة أسفل السيليكون في الجدول الدوري ، لدينا الجرمانيوم المعدني مع عدد ذري من 32.
الجرمانيوم أكثر وفرة من المعادن الأخرى ، مثل الزرنيخ والأنتيمون. ومع ذلك ، لها تفاعلية عالية مع عناصر أخرى يعني أنه لم يتم العثور عليه في شكله الأولي في الطبيعة. في درجة حرارة الغرفة ، لدى Germanium بنية صلبة وهشة ولا تتفاعل مع الهواء. ومع ذلك ، مع زيادة درجة الحرارة ، تزداد تفاعلها أيضًا ، مما يؤدي إلى تكوين أكاسيد في حوالي 600-700 درجة مئوية (1000-1100 درجة فهرنهايت).
يستخدم الجرمانيوم أيضًا في تطبيقات أشباه الموصلات ، على الرغم من أنه إلى حد أقل من السيليكون. بالإضافة إلى ذلك ، لديها تطبيقات في الطب والعملة المعدنية.
الزرنيخ (AS)
الزرنيخ العنصر الكيميائي ، الذي ينتمي إلى المجموعة 15 ولديه عدد ذري يبلغ 33 الطبيعة السامة. في درجة حرارة الغرفة ، يكون الزرنيخ مستقرًا ولا يتفاعل مع الهواء. ومع ذلك ، في وجود الرطوبة ، يتأكسد لتشكيل تشويه برونزي ذهبي يتحول في النهاية إلى اللون الأسود.
يمكن أن يؤدي التعرض طويل الأجل للزرنيخ من خلال الطعام والماء إلى أمراض خطيرة ، بما في ذلك السرطان. ومع ذلك ، تجدر الإشارة إلى أن الزرنيخ هو عنصر تتبع أساسي لبعض الكائنات الحية. إنه يلعب دورًا مباشرًا وغير مباشر في إنتاج كل من العوامل البيولوجية المفيدة والضارة.
يستخدم الزرنيخ أيضًا في قطاعات أخرى مثل تصنيع الزجاج وإنتاج أشباه الموصلات والمواد الكيميائية الزراعية والتعدين.
الأنتيمون (SB)
تم العثور على أنتيمون ، مع الرقم الذري 51 ، في المجموعة 15 من الجدول الدوري ، مباشرة أسفل الزرنيخ. لديها هيكل صعب وهش، التي تتميز بمظهر فضي.
يتم استخراج معظم الأنتيمون من المعادن الكبريتيد ، والستيبنيت ، مع الصين وروسيا وبوليفيا وقيرغيزستان التي تحمل غالبية محميات الأنتيمون. إلى جانب ذلك ، تعد الصين أكبر منتج لأنتيمون في العالم.
وقد تم استخدام Antimony تقليديًا في التطبيقات الطبية والتجميلية. مع مرور الوقت ، أصبح أيضًا ذا قيمة في إنتاج مواد ، والدهانات ، والبطاريات ، والزجاج ، والفخار ، ووسائط التخزين البصرية ، وأجهزة أشباه الموصلات مثل الثنائيات وكاشفات الأشعة تحت الحمراء.
بالنسبة لأوروبا والولايات المتحدة ، تعد Antimony عنصرًا مهمًا ، حيث يتم استيراد 100 ٪ منها. يمكن أن يؤثر اضطراب العرض بشدة على الصناعات الأساسية مثل السيارات والبناء والدفاع.
تيلوريوم (TE)
Tellurium هو معدني نادر وأبيض فضي تم اكتشافه لأول مرة في مناجم الذهب مثل الذهب الذهب (ويعرف أيضًا باسم Calaverite). بوفرة جزء واحد لكل مليار (1 ميكروغرام لكل كيلوغرام) ، تيلوريوم هو نادر مثل البلاتين.
لم يتم تحديد أي تطبيقات واسعة النطاق من tellurium حتى الآن. في الصناعة ، يستخدم Tellurium في المقام الأول كعنصر لصنع السبائك وفي إنتاج الألواح الشمسية والأجهزة الحرارية.
البولونيوم (PO)
البولونيوم هو المعادن المشعة يتم تصنيف ذلك أحيانًا على أنه ميتولويد. لديها 42 نظير ، لا شيء مستقر وكلها مشعة. يتراوح عمر نظائر البولونيوم من 115 نانو ثانية (مليار من الثانية) لـ PO-205M4 إلى 124 عامًا لـ PO-201.
يحتوي Polonium على العديد من التطبيقات ، وكلها تستخدم خصائصها المشعة. بعض هذه هي:
- كمولد حراري كهروإجهادي لضوء الفضاء
- كجهاز مضاد للاختراق للتخلص من الشحنة الثابتة
- كمصدر للنيوترون بالاشتراك مع البريليوم
أستاتين (في)
ومع ذلك ، يتم تصنيف الأستاتين على أنه معدني ، ومع ذلك ، بعض التصنيفات تصنفها على أنها غير محدودة. إنه العنصر الثاني إلى الأخير في مجموعة الهالوجين ، يسبقه الفلور والكلور والبروم واليود ، ويظهر العديد من الخصائص الشائعة مع هذه العناصر.
أستاتين هو مشعة للغاية، وخصائصها لم تتم دراستها بالتفصيل ، حيث لم يتم تصنيعها أبدًا بكميات كافية لتحليل شامل. علاوة على ذلك ، فإنه يسمع بسرعة بحيث يمكنك أن تفقد نصفه في غضون ساعة.
Astatine لديه تطبيقات محدودة بسبب النشاط الإشعاعي ونصف العمر القصير. ومع ذلك ، فقد تم استخدامه في الأبحاث ، في المقام الأول باعتباره تتبع مشع وفي علاج سرطان الغدة الدرقية.
خاتمة
المعادن هي مجموعة مهمة من العناصر التي سد الفجوة بين المعادن وغير المعادن. يتيح مزيجهم من خصائص المعادن وغير المعدنية استخدامها في الصناعات المتنوعة للغاية ، من الزراعة إلى التخزين البصري والالإيجابي الضوئي.
خصائصها شبه الموصل ، على وجه الخصوص ، لها تقنية متطورة بشكل كبير والحوسبة الحديثة. بعض المعادن ، مثل الزرنيخ ، سامة ، ومع ذلك ، فإن استخدامها الخاضع للرقابة يوفر فوائد لا مثيل لها في مختلف القطاعات.
بسبب الأسباب المذكورة أعلاه ، من المتوقع أن ينمو الطلب على المعادن. لكن، لقد جعلتها ندرة بعض المعادن. على سبيل المثال ، ينخفض إنتاج Antimony لأن المصادر الحالية تستنفد بسرعة ، مع عدم اكتشاف بدائل جديدة.
هذا جعل من الأهمية بمكان تحديد المصادر المستدامة للمعادن. الجهود جارية للبحث والاحتفاظ وإعادة تدوير المعادن.
انضم إلى منتدى المصممين
خبرتك ضرورية للمجتمع. انضم إلينا وساهم بمعرفتك
انضم إلى المنتدى الآنشارك وتعلّم وتقدّم مع أفضل المحترفين في هذا المجال

